Un nouveau système d’imagerie par résonance magnétique (IRM) spécifiquement conçu pour les nouveau-nés vient d’obtenir l’autorisation de la Food and Drug Administration (FDA) américaine. Cet appareil, développé par Eyas Medical Imaging, promet d’améliorer significativement les diagnostics et les soins prodigués aux bébés.
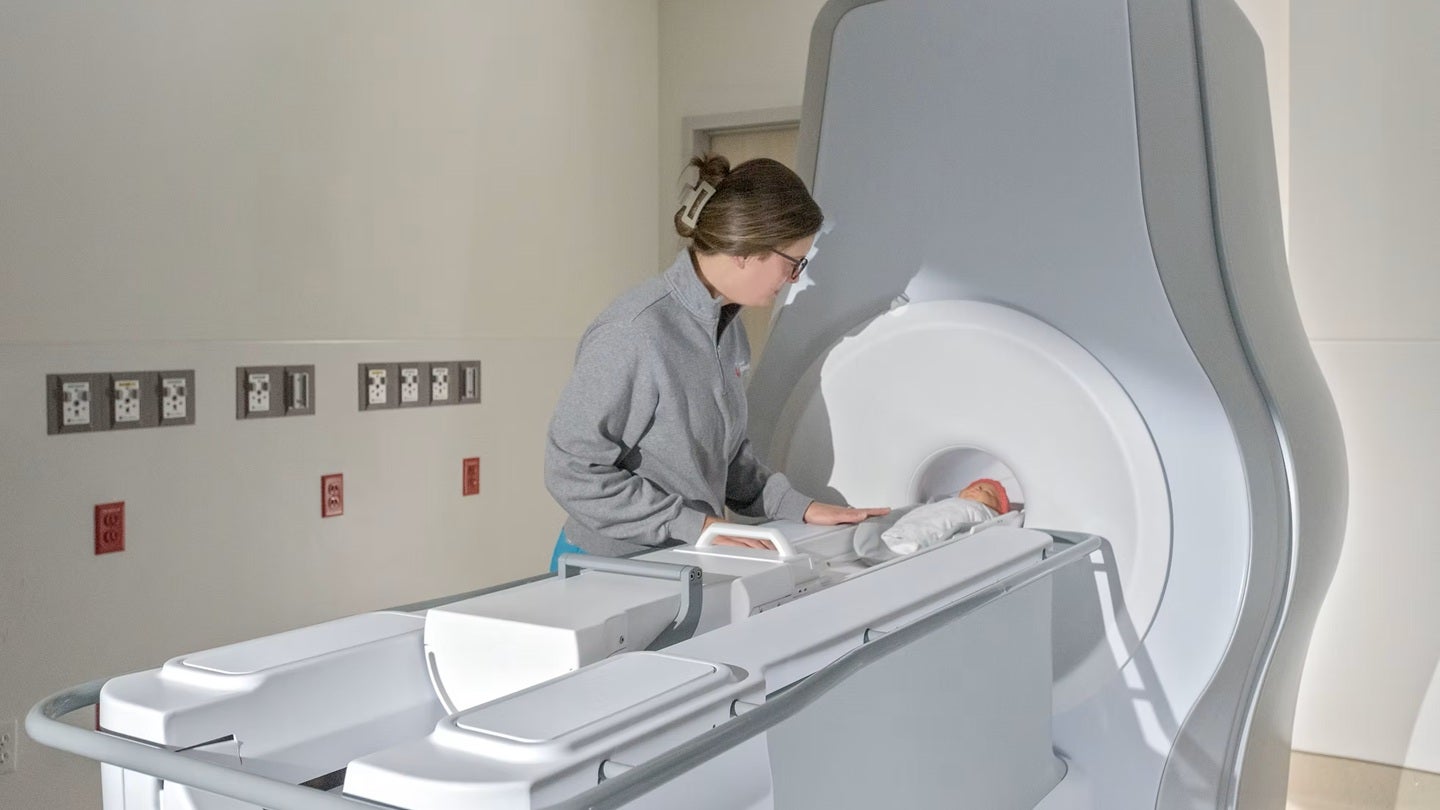
L’Ascent³ᵀ est le premier système IRM à champ élevé de trois Tesla (3T) entièrement dédié à l’imagerie néonatale et infantile. Il permet d’obtenir des images détaillées des organes vitaux, tels que le cœur, les poumons, l’abdomen et le cerveau, avec une précision accrue.
Jusqu’à présent, les médecins étaient contraints d’utiliser des appareils IRM conçus pour les adultes, ce qui posait des difficultés pour l’examen des nouveau-nés. L’Ascent³ᵀ répond à ce problème en offrant une solution adaptée à leur anatomie fragile et à leurs besoins spécifiques.
Un des principaux défis en matière d’IRM néonatale résidait dans la nécessité de transporter les nourrissons, souvent très vulnérables, des unités de soins intensifs néonatals (USIN) vers des salles d’examen IRM éloignées. Le système Ascent³ᵀ, grâce à sa conception compacte, peut être installé directement au sein de l’USIN, éliminant ainsi ce transfert potentiellement risqué.
Par ailleurs, cet appareil fonctionne avec une consommation d’hélium quasi nulle, ce qui simplifie considérablement sa maintenance et son fonctionnement. Il ne nécessite ni tuyau de trempe, ni système de ventilation externe.
Le développement de l’Ascent³ᵀ s’appuie sur plus de 1 500 IRM de nourrissons réalisées à titre expérimental au Cincinnati Children’s Hospital. Il intègre une table patient amovible qui peut également servir de moyen de transport, facilitant ainsi la logistique au sein de l’USIN. La technologie embarquée comprend également un logiciel d’exploitation, une électronique avancée et des séquences d’impulsions développées par Philips Medical Systems Nederland.
« L’autorisation 510(k) représente une étape cruciale pour notre entreprise et témoigne de notre engagement à fournir aux professionnels de la santé les outils nécessaires pour sauver davantage de vies de bébés grâce à une imagerie de pointe », a déclaré Matt Storer, président-directeur général d’Eyas Medical Imaging.
Eyas Medical Imaging prévoit de lancer la commercialisation de l’Ascent³ᵀ aux États-Unis dans les prochains mois. Sa disponibilité dans d’autres pays n’a pas encore été annoncée.