Publié le 26 février 2026 04:04:00. Des chercheurs australiens ont mis en lumière le mécanisme d’action de plusieurs antibiotiques expérimentaux sur la bactérie responsable de la tuberculose, ouvrant de nouvelles perspectives pour lutter contre cette maladie infectieuse mondiale et les souches résistantes aux traitements.
- Une étude révèle comment trois composés naturels perturbent une machine moléculaire essentielle à la survie de Mycobacterium tuberculosis.
- Ces composés n’arrêtent pas le système de recyclage bactérien, mais interfèrent avec lui de manière distincte, provoquant des déséquilibres généralisés.
- La recherche identifie le complexe ClpC1 – ClpP1P2 comme une cible médicamenteuse prometteuse, encore relativement sous-explorée.
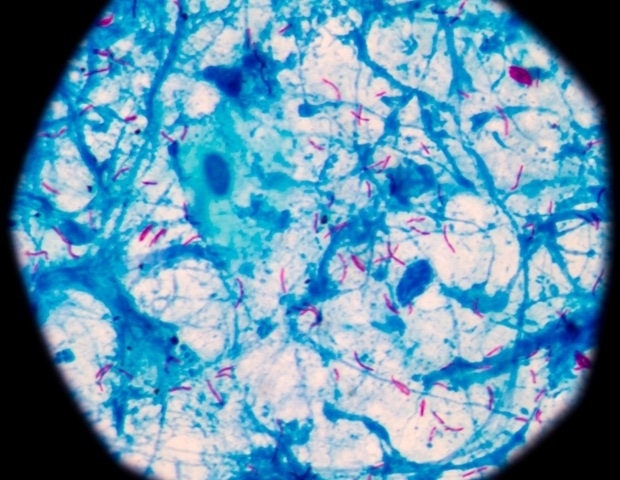
La tuberculose (TB) demeure un problème de santé publique majeur à l’échelle mondiale, causant environ 1,2 million de décès chaque année. La propagation de souches pharmacorésistantes, en particulier dans la région Asie-Pacifique, souligne l’urgence de développer de nouvelles stratégies thérapeutiques. Une équipe de l’Université de Sydney et du Centenary Institute a étudié l’impact de trois antibiotiques naturels – l’écumicine, l’ilamycine et la cyclomarine – sur une composante vitale de la bactérie Mycobacterium tuberculosis.
Cette composante, connue sous le nom de complexe ClpC1 – ClpP1P2, est une machine moléculaire qui permet à la bactérie de décomposer les protéines endommagées ou inutiles, un processus essentiel à sa survie et à son adaptation au stress. Sans ce système de recyclage, la bactérie tuberculeuse ne peut survivre, ce qui en fait une cible thérapeutique intéressante.
Le professeur Warwick Britton, co-auteur principal et chef de laboratoire au Centre d’infection et d’immunité du Centenary Institute, explique que l’étude révèle une complexité insoupçonnée dans la manière dont ces antibiotiques affectent ce système :
« Les bactéries tuberculeuses dépendent de ce système de recyclage pour rester en vie, en particulier dans des conditions stressantes à l’intérieur du corps humain. Nos résultats montrent que ces composés n’arrêtent pas simplement le système. Au lieu de cela, chacun interfère avec lui de manière différente, déclenchant des déséquilibres généralisés dans l’ensemble de la bactérie. Cette perturbation affaiblit sa capacité à fonctionner et à survivre. »
Warwick Britton, professeur et chef de laboratoire
La première auteure, Isabel Barter, doctorante à l’Université de Sydney, a mené une partie de l’étude au Centenary Institute. Elle a précisé que l’équipe a mesuré les changements survenus dans plus de 3 000 protéines au sein de Mycobacterium tuberculosis.
« En suivant les changements dans la majeure partie du réseau protéique de la bactérie, nous avons pu voir comment la perturbation d’un seul complexe essentiel peut remodeler l’ensemble du paysage protéique interne de la bactérie. Cette compréhension plus approfondie nous donne des informations précieuses sur la manière dont nous pourrions affiner ces composés et concevoir des traitements antituberculeux plus précis et plus efficaces. »
Isabel Barter, doctorante
Le professeur Richard Payne, co-auteur principal de l’Université de Sydney, souligne que le complexe ClpC1 – ClpP1P2 représente une cible médicamenteuse prometteuse, mais encore sous-exploitée. DOI: 10.1038/s41467-026-68423-2
« Notre étude met en évidence le potentiel de cibler directement ce système de dégradation des protéines. En comprenant comment différents composés interagissent avec lui et perturbent son fonctionnement normal, nous pouvons concevoir de manière plus stratégique la prochaine génération de médicaments antituberculeux. »
Richard Payne, professeur
L’équipe de recherche estime que cette étude constitue une avancée significative dans le développement de nouvelles options thérapeutiques contre la tuberculose, y compris les formes résistantes aux médicaments actuellement disponibles.