Publié le 24 février 2026 à 01h15. Une nouvelle étude met en lumière un mécanisme moléculaire impliqué dans le développement de la bronchopneumopathie chronique obstructive (BPCO), ouvrant la voie à de potentielles nouvelles stratégies thérapeutiques ciblant l’inflammation pulmonaire.
- L’exposition aux particules fines en suspension dans l’air, combinée à la fumée de cigarette, accélère la progression de la BPCO.
- Une kinase appelée CK2 et un facteur de liaison appelé CTCF jouent un rôle clé dans ce processus en modifiant l’activité des macrophages pulmonaires.
- La gaylussacine, un stilbénoïde, s’est révélée prometteuse pour inhiber cette voie inflammatoire et atténuer les symptômes de la BPCO chez des modèles animaux.
La bronchopneumopathie chronique obstructive (BPCO), une maladie pulmonaire caractérisée par une bronchite chronique et un emphysème, représente un problème de santé publique majeur. En 2020, elle était la sixième cause de décès aux États-Unis. Si les traitements actuels peuvent soulager les symptômes, ils n’enrayent que rarement la progression de la maladie. La fumée de cigarette reste le principal facteur de risque, mais l’exposition aux particules en suspension (PM) contribue également de manière significative, agissant en synergie avec la fumée pour aggraver l’atteinte pulmonaire.
Les macrophages, des cellules immunitaires présentes dans les poumons, jouent un rôle central dans la pathogenèse de la BPCO. Leur dérégulation entraîne une inflammation chronique et une destruction tissulaire, via la libération excessive de cytokines, d’espèces réactives de l’oxygène et de l’azote (ROS/RNS) et de protéases. Des recherches récentes ont montré que l’exposition aux particules induit une infiltration de macrophages dans les poumons, modifiant l’expression de certains gènes impliqués dans la voie métabolique de la kynurénine (KP). Ces modifications réduisent la production de NAD+, inactive la protéine SIRT1 et favorisent l’expression de gènes pro-inflammatoires.
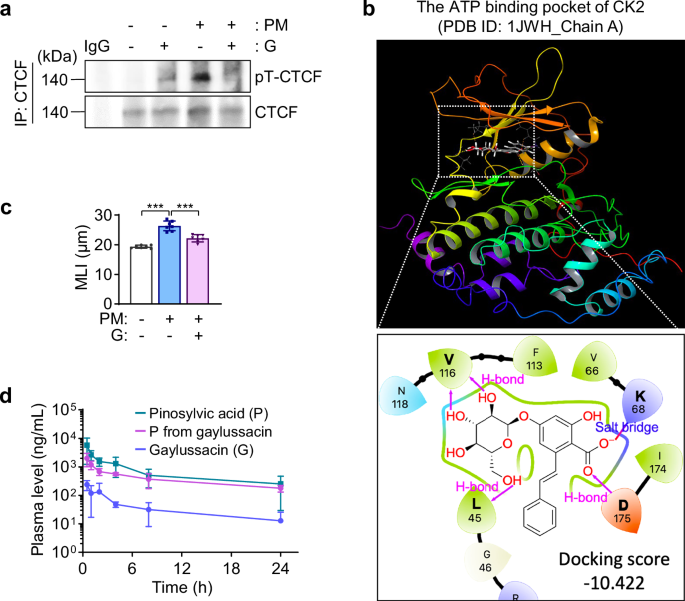
Une étude approfondie a révélé que l’activation du facteur de liaison CCCTC (CTCF) est un élément clé de ce processus. Les chercheurs ont identifié une kinase, CK2, comme étant responsable de l’activation de CTCF. En effet, l’exposition aux particules induit une accumulation de CK2 dans le noyau des macrophages, entraînant la phosphorylation de CTCF et son association avec des protéines de cohésine. Cette interaction modifie la liaison de CTCF à l’ADN, exacerbant l’inflammation. L’inhibition de CK2 par le silmitasertib a permis de restaurer l’expression des enzymes de la voie KP et de réduire l’inflammation.
Pour identifier des composés capables d’inhiber cette voie inflammatoire, les chercheurs ont criblé plusieurs stilbénoïdes. La gaylussacine et le ptérostilbène se sont avérés particulièrement efficaces pour bloquer la liaison de CTCF à l’ADN. La gaylussacine a également démontré une capacité à réduire la production de ROS et de NO sans toxicité significative pour les cellules saines. Des tests plus poussés ont révélé que la gaylussacine inhibe directement l’activité de CK2, empêchant ainsi la phosphorylation de CTCF et la formation du complexe CTCF-cohésine. Des analyses de données de séquençage d’ARN unicellulaire provenant de patients atteints de BPCO ont confirmé une expression altérée des gènes cibles de CTCF dans les macrophages de ces patients.
Des expériences sur des modèles animaux de BPCO induite par les particules ont montré que le traitement à la gaylussacine atténue l’inflammation pulmonaire, réduit l’hypertrophie alvéolaire, prévient l’apoptose et diminue la production de cytokines pro-inflammatoires. L’analyse pharmacocinétique a révélé que la gaylussacine est métabolisée en acide pinosylvique, qui présente une meilleure stabilité et biodisponibilité. Les deux composés se sont avérés bien tolérés et efficaces pour atténuer la progression de la BPCO.
Ces résultats suggèrent que la gaylussacine pourrait représenter une nouvelle approche thérapeutique prometteuse pour lutter contre l’inflammation chronique associée à la BPCO, tant chez les fumeurs que chez les non-fumeurs. Des études complémentaires sont nécessaires pour évaluer son efficacité et sa sécurité chez l’homme, ainsi que pour déterminer le rôle précis de CTCF dans la pathogenèse de la BPCO. Plus d’informations sur les particules en suspension et sur le lien entre particules et MPOC.