Publié le 2025-10-07 09:33:00. Une enzyme clé dans la progression du cancer du sein triple négatif (TNBC) a été identifiée, ouvrant la voie à de nouvelles stratégies thérapeutiques. Des chercheurs de Weill Cornell Medicine ont découvert que le blocage de l’enzyme EZH2 pourrait stopper la propagation de ce cancer agressif en restaurant la division cellulaire normale.
- Une enzyme, EZH2, favorise la division cellulaire anormale et les métastases dans le cancer du sein triple négatif.
- Le blocage de cette enzyme avec des médicaments existants pourrait restaurer la division cellulaire et empêcher la propagation du cancer.
- Cette découverte remet en question les approches traditionnelles visant à induire la mort cellulaire par l’instabilité chromosomique.
Le cancer du sein triple négatif (TNBC) est l’une des formes les plus redoutables de cancer du sein, caractérisée par son agressivité et ses difficultés de traitement. Une nouvelle étude menée par Weill Cornell Medicine propose une stratégie potentiellement révolutionnaire pour en freiner la progression. Les scientifiques ont identifié une enzyme, l’EZH2, comme étant le moteur d’une division cellulaire déréglée dans les cellules TNBC, leur permettant de former des métastases dans des organes distants. Des expériences précliniques ont démontré qu’en bloquant l’EZH2, il est possible de rétablir un comportement cellulaire normal et d’endiguer la dissémination des cellules cancéreuses.
« Les métastases sont la principale raison pour laquelle les patientes atteintes d’un cancer du sein à triple négatif font face à de faibles chances de survie », a déclaré le Dr Vivek Mittal, professeur de recherche Ford-Isom en chirurgie cardiothoracique et membre du Sandra et Edward Meyer Cancer Center à Weill Cornell Medicine. « Notre étude suggère une nouvelle approche thérapeutique pour bloquer les métastases avant même leur apparition et aider les patients à surmonter ce cancer mortel. »
Dr Vivek Mittal, professeur, Weill Cornell Medicine
Ces conclusions remettent en cause l’idée selon laquelle les traitements anticancéreux devraient exacerber les erreurs de division cellulaire pour provoquer la mort des cellules tumorales. En temps normal, lors de la division cellulaire, les chromosomes sont dupliqués et partagés équitablement entre deux cellules filles. Or, dans de nombreuses cellules cancéreuses, ce processus est défaillant, entraînant une instabilité chromosomique.
« Je trouve la tentative de pousser les cellules cancéreuses au-delà du point de rupture avec davantage d’instabilité chromosomique quelque peu préoccupante, car si l’on n’atteint pas le bon niveau, cela peut paradoxalement entraîner une maladie agressive », a précisé le Dr Mittal. « Nos résultats suggèrent au contraire que le rétablissement de l’ordre dans la division cellulaire en ciblant l’EZH2 peut les empêcher de se propager. »
Dr Vivek Mittal, professeur, Weill Cornell Medicine
L’épigénétique au cœur des métastases
Environ 5 % des cellules d’une tumeur primaire de TNBC sont particulièrement aptes à métastaser. Ces cellules présentent des caractéristiques distinctives, telles qu’un métabolisme altéré, une instabilité chromosomique accrue et des modifications épigénétiques – des altérations de l’ADN ou des protéines associées qui ne modifient pas directement le code génétique.
L’équipe du Dr Mittal a identifié l’EZH2 comme un acteur majeur des métastases dans ces cellules. Normalement, l’EZH2 régule la manière dont l’ADN est organisé au sein des cellules. Cependant, en cas de cancer, l’EZH2 est souvent surproduit, ce qui conduit à la mise en silence de gènes essentiels à la ségrégation correcte des chromosomes et déclenche des erreurs lors de la division cellulaire.
Environ 5 % des cellules d’une tumeur primaire de TNBC sont particulièrement aptes à métastaser.
L’analyse des données de patients, menée par le Dr Shelley Yang Bai, associée postdoctorale en chirurgie cardiothoracique à Weill Cornell Medicine, a révélé une corrélation entre des niveaux plus élevés d’EZH2 et une instabilité chromosomique accrue dans les cellules tumorales. Des expériences en laboratoire ont confirmé ces observations : l’inhibition de l’EZH2 par le tazemétostat, un médicament déjà approuvé par la FDA pour certains cancers, a réduit l’instabilité chromosomique dans des lignées cellulaires de TNBC. Inversement, l’augmentation génétique des niveaux d’EZH2 a entraîné une multiplication des erreurs de division.
Des modèles murins présentant des niveaux élevés d’EZH2 ont montré une augmentation des métastases pulmonaires par rapport aux tumeurs dépourvues de cette enzyme, confirmant ainsi le lien direct entre EZH2, l’instabilité chromosomique et la formation de métastases.
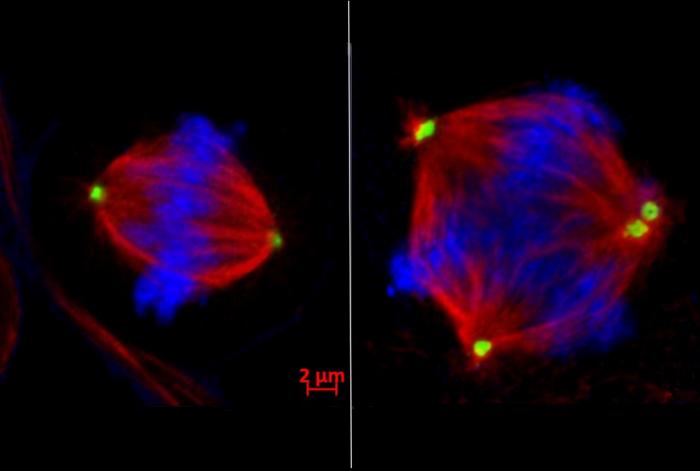
À gauche : Division cellulaire normale avec les chromosomes (en bleu) alignés et prêts à être séparés en deux cellules filles par les centrosomes (en vert). À droite : lors d’une division cellulaire défectueuse, la présence excessive de centrosomes conduit à la formation de plusieurs cellules souffrant d’instabilité chromosomique. Crédit : Dr Shelly Yang Bai
Le chaos chromosomique décrypté
L’équipe de recherche a découvert que l’EZH2 entraîne la répression du gène tankyrase 1, qui assure normalement le bon fonctionnement des mécanismes de séparation des chromosomes. Cette répression déclenche une réaction en chaîne : la diminution des niveaux de Tankyrase 1 provoque une accumulation excessive de CPAP, une protéine qui régule les centrosomes. L’emballement de la multiplication des centrosomes conduit les cellules à se diviser de manière erronée en trois cellules filles, voire plus.
L’inhibition de l’EZH2 a permis de rétablir l’équilibre dans la division cellulaire et de réduire significativement les métastases dans les modèles précliniques. « Pour la première fois, nous avons établi un lien mécanistique entre EZH2, un régulateur épigénétique, et l’instabilité chromosomique », a souligné le Dr Bai.
Cette étude propose une nouvelle approche prometteuse pour traiter le cancer du sein triple négatif en s’attaquant à la cause profonde des métastases.
« Cette étude propose une nouvelle approche prometteuse pour traiter le cancer du sein triple négatif en s’attaquant à la cause profonde des métastases », a affirmé le Dr Magdalena Plasilova, professeure agrégée de chirurgie clinique et oncologue chirurgicale au New York-Presbyterian / Weill Cornell Medical Center. « Je constate de visu l’impact dévastateur des métastases sur les patients, et cette découverte apporte de l’espoir pour l’amélioration des pronostics et des taux de survie. »
Dr Magdalena Plasilova, professeure, New York-Presbyterian / Weill Cornell Medical Center
Le tazemétostat pourrait ainsi potentiellement être repositionné comme traitement du TNBC, bien que d’autres médicaments puissent offrir des effets similaires, voire supérieurs. « Notre découverte ouvre la voie à des essais cliniques visant à évaluer les inhibiteurs de l’EZH2 dans le cancer du sein à haut risque et potentiellement dans d’autres cancers également marqués par une instabilité chromosomique, comme l’adénocarcinome pulmonaire », a conclu le Dr Mittal.
Prochaines étapes et perspectives
En établissant un lien entre cette enzyme et l’instabilité chromosomique, les chercheurs ont identifié une cible thérapeutique prometteuse capable de prévenir la dissémination du cancer. Avec des inhibiteurs de l’EZH2 tels que le tazemétostat ayant déjà démontré leur efficacité dans des modèles précliniques, cette découverte pourrait mener à des essais cliniques visant à améliorer les résultats et la survie des patientes confrontées à cette forme agressive de cancer du sein.