Publié le 17 février 2026. Une nouvelle étude de l’UT Southwestern Medical Center révèle que les mutations du gène KRAS, fréquemment impliquées dans le cancer du poumon, ne se comportent pas toutes de la même manière, ce qui pourrait ouvrir la voie à des traitements plus personnalisés.
- Différents types de mutations du gène KRAS influencent la réponse immunitaire des cellules cancéreuses.
- La mutation G12D semble moins susceptible d’attirer les cellules immunitaires et présente des niveaux plus faibles de PDL1.
- Une combinaison d’inhibiteurs spécifiques à la mutation G12D et d’inhibiteurs de points de contrôle immunitaires pourrait améliorer considérablement les résultats pour les patients.
Dallas, Texas – Des chercheurs de l’UT Southwestern Medical Center ont mis en évidence des différences significatives dans la manière dont les différents types de mutations du gène KRAS affectent l’interaction entre les cellules cancéreuses et le système immunitaire. KRAS est l’oncogène le plus fréquemment muté dans tous les cancers humains, et ces découvertes, publiées dans Science Translational Medicine, pourraient révolutionner l’approche thérapeutique du cancer du poumon.
Jusqu’à un tiers des patients atteints d’adénocarcinome du poumon, la forme la plus courante de cette maladie, présentent des mutations du gène KRAS. Parmi ceux-ci, environ 41 % présentent une mutation de type G12C, tandis que 17 % présentent une mutation G12D. Bien que ces mutations aient longtemps été considérées comme ayant des effets similaires sur le développement et la progression tumorale, l’étude révèle que les tumeurs porteuses de la mutation G12C répondent généralement mieux aux inhibiteurs de points de contrôle immunitaires que celles porteuses de la mutation G12D.
Pour comprendre les raisons de cet écart, l’équipe du Dr Esra Akbay a mené des expériences sur des souris porteuses de ces mutations. Les résultats ont montré que le cancer progressait beaucoup plus rapidement chez les souris porteuses de la mutation G12D, et que leur espérance de vie était significativement réduite. L’analyse de vastes bases de données de patients atteints de cancer a confirmé ces observations, révélant que les personnes porteuses de la mutation G12D étaient souvent diagnostiquées plus tôt, suggérant une croissance tumorale plus rapide.
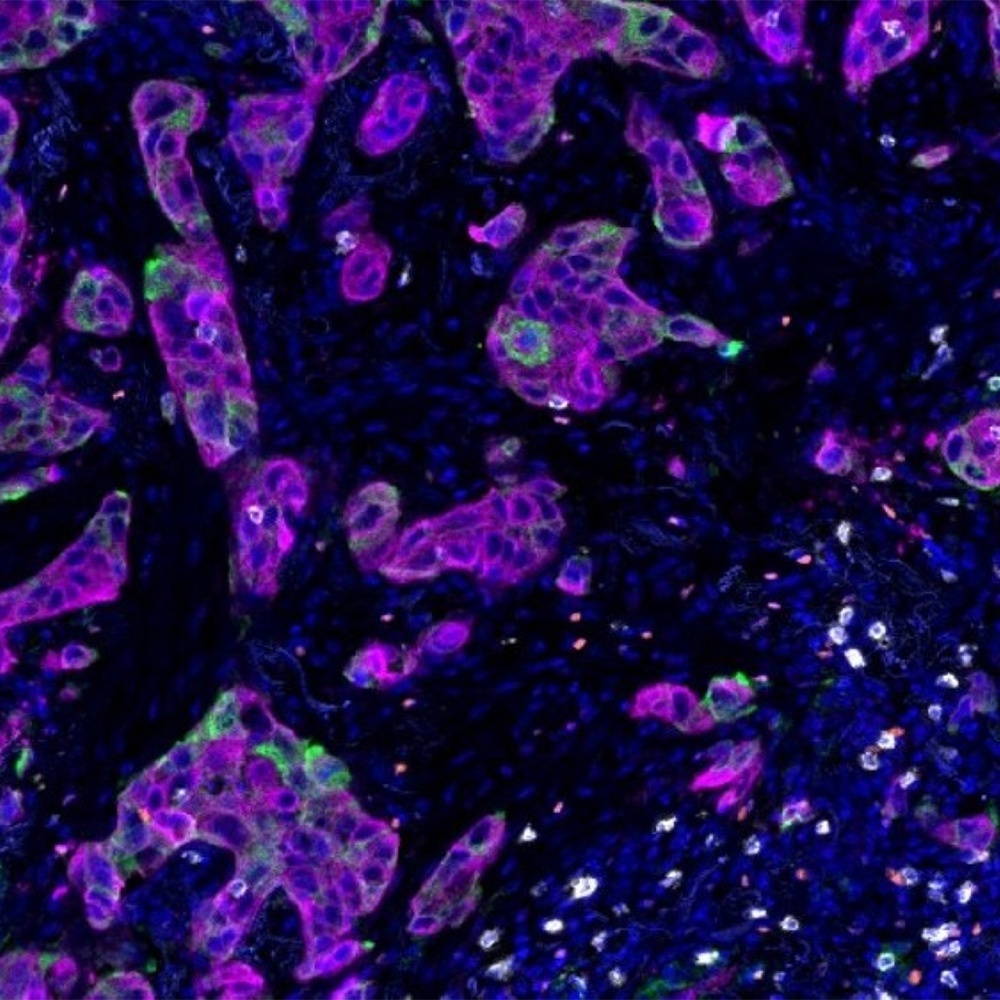
Une analyse plus approfondie des tumeurs a révélé que les gènes associés à l’inflammation et à l’activité immunitaire étaient plus actifs chez les souris porteuses de la mutation G12C. Ces tumeurs contenaient également davantage de cellules immunitaires, notamment des lymphocytes et des cellules T cytotoxiques, ainsi que des niveaux plus élevés de PDL1, la protéine ciblée par les inhibiteurs de points de contrôle immunitaires. De plus, elles produisaient davantage d’antigènes, des molécules qui signalent la présence de cellules cancéreuses au système immunitaire.
Les chercheurs ont ensuite testé l’efficacité de médicaments ciblant spécifiquement chaque type de mutation. Si toutes les souris ont initialement répondu aux traitements, celles porteuses de la mutation G12D ont rechuté plus rapidement que celles porteuses de la mutation G12C. Cependant, en combinant un médicament ciblant spécifiquement la mutation G12D avec un inhibiteur de point de contrôle immunitaire, les chercheurs ont observé une réponse complète chez de nombreuses souris, indiquant une éradication totale de la tumeur.
« Plutôt que de considérer KRAS comme une entité unique, cette étude recadre le domaine en posant une question plus précise : « Quel type de mutation KRAS ? » Nous montrons que différents types de mutations créent des écosystèmes tumoraux distincts qui peuvent avoir des effets réels sur les résultats pour les patients. »
Esra Akbay, Ph.D., professeure agrégée de pathologie et membre du Harold C. Simmons Comprehensive Cancer Center de l’UT Southwestern.
Ces résultats suggèrent que le type de mutation KRAS joue un rôle crucial dans le comportement des cellules cancéreuses et dans la réponse immunitaire. Identifier précisément la mutation présente chez chaque patient pourrait permettre de concevoir des plans de traitement personnalisés, combinant des inhibiteurs spécifiques à la mutation et des inhibiteurs de points de contrôle immunitaires, afin d’améliorer le pronostic.
L’étude a été financée par des subventions du Cancer Prevention and Research Institute of Texas (CPRIT Scholar Award RR160080), des National Institutes of Health (NIH) (R01CA289500, R01CA276058), du National Cancer Institute (NCI) UT Southwestern-MD Anderson Cancer Center Specialized Program of Research Excellence (SPORE) (5P50CA070907), de l’American Cancer Society Research Scholar Award (RSG-22-051-01-IBCD), de la Fondation Forbeck et d’une subvention de soutien au NCI Cancer Center (P30CA142543).
D’autres chercheurs de l’UTSW ayant contribué à cette étude incluent Hai-Cheng Huang, Ph.D., et Qing Deng, Ph.D., du Laboratoire Akbay; Luis De Las Casas, MD, professeur de pathologie ; Lin Xu, Ph.D., professeur adjoint à l’École de santé publique Peter O’Donnell Jr. et de Pédiatrie; et Lei Guo, Ph.D., biologiste computationnel.
Le Dr Akbay est membre du programme de développement et de recherche sur le cancer du Simmons Cancer Center.
À propos du centre médical UT Southwestern : UT Southwestern, l’un des principaux centres médicaux universitaires du pays, intègre une recherche biomédicale de pointe avec des soins cliniques et une éducation exceptionnels. Les professeurs de l’institution ont reçu six prix Nobel et comprennent 24 membres de l’Académie nationale des sciences, 25 membres de l’Académie nationale de médecine et 13 chercheurs du Howard Hughes Medical Institute. Le corps professoral à temps plein, composé de plus de 3 300 personnes, est à l’origine de progrès médicaux révolutionnaires et s’engage à traduire rapidement la recherche scientifique en nouveaux traitements cliniques. Les médecins de l’UT Southwestern dans plus de 80 spécialités soignent plus de 143 000 patients hospitalisés, s’occupent de plus de 470 000 cas aux urgences et supervisent près de 5,3 millions de visites ambulatoires par an.