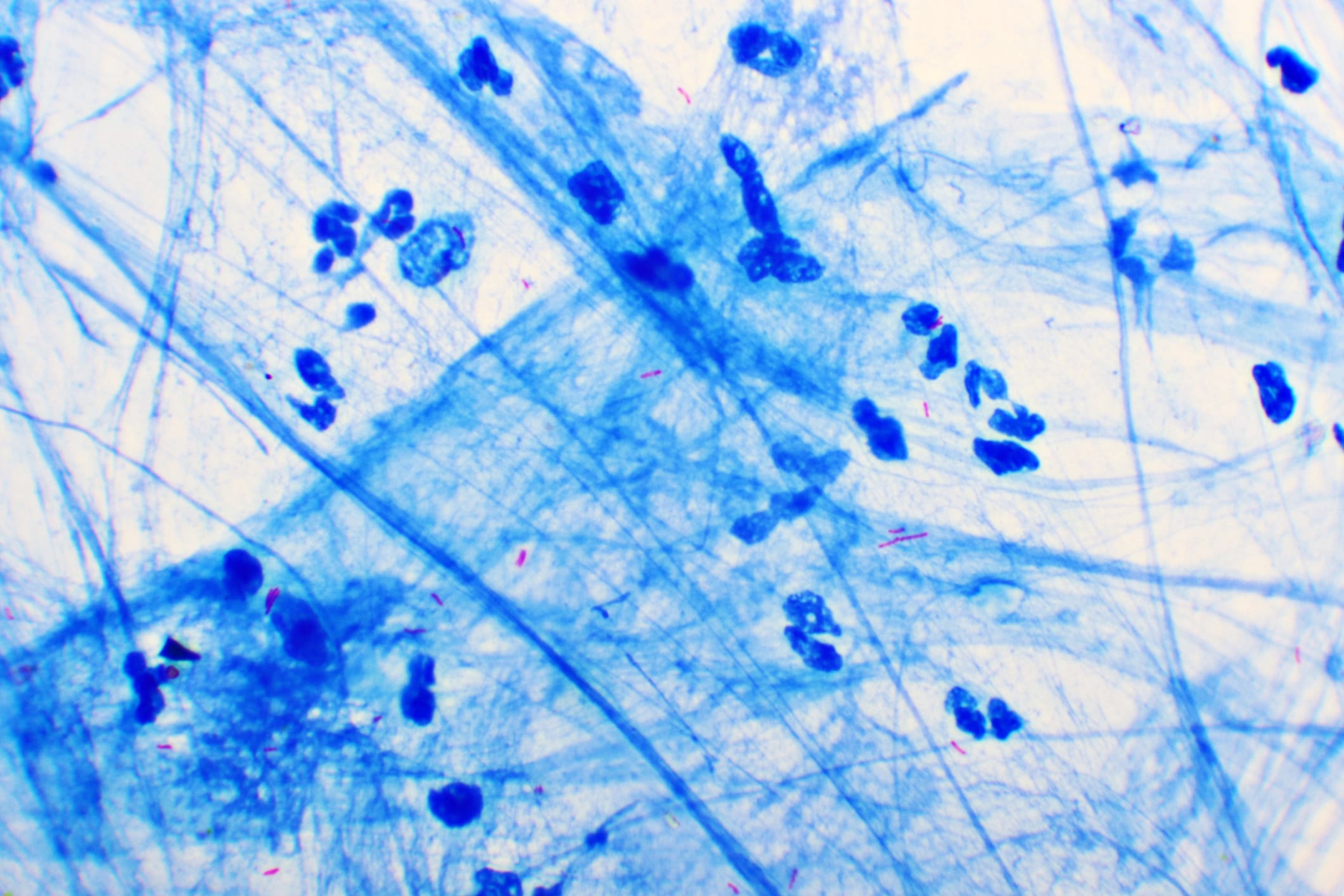
Publié le 21 février 2026 à 14h06. Des chercheurs ont mis en évidence une stratégie de survie sophistiquée employée par les bactéries responsables de la tuberculose : la modification de la structure des membranes cellulaires de l’hôte pour échapper à la destruction par le système immunitaire. Cette découverte ouvre de nouvelles perspectives pour le développement de traitements plus efficaces contre cette maladie infectieuse mondiale.
- Les mycobactéries libèrent des vésicules extracellulaires contenant des lipides qui rigidifient les membranes des cellules immunitaires, bloquant ainsi le processus de destruction bactérienne.
- Cette étude révèle un mécanisme d’évasion immunitaire basé sur les lipides, démontrant que ces derniers peuvent altérer les membranes cellulaires et affaiblir les défenses immunitaires, même dans les cellules non infectées.
- L’identification de la production de vésicules et du renforcement membranaire comme outils de survie bactérienne suggère de nouvelles cibles thérapeutiques pour lutter contre la tuberculose.
La tuberculose, qui tue plus d’un million de personnes chaque année, représente un défi majeur de santé publique, en particulier en Asie, en Afrique et en Amérique latine. Les mycobactéries, agents pathogènes responsables de cette maladie, ont développé des mécanismes complexes pour déjouer les cellules immunitaires humaines et éviter leur destruction.
« J’ai grandi dans un État indien où les épidémies de tuberculose sont un problème majeur et j’ai toujours été curieux de comprendre comment ces maladies se propagent », explique Ayush Panda, ancien étudiant diplômé du laboratoire de Mohammed Saleem à l’Institut national d’enseignement et de recherche scientifiques en Inde. « C’est ce qui m’a motivé à mener ces recherches. »
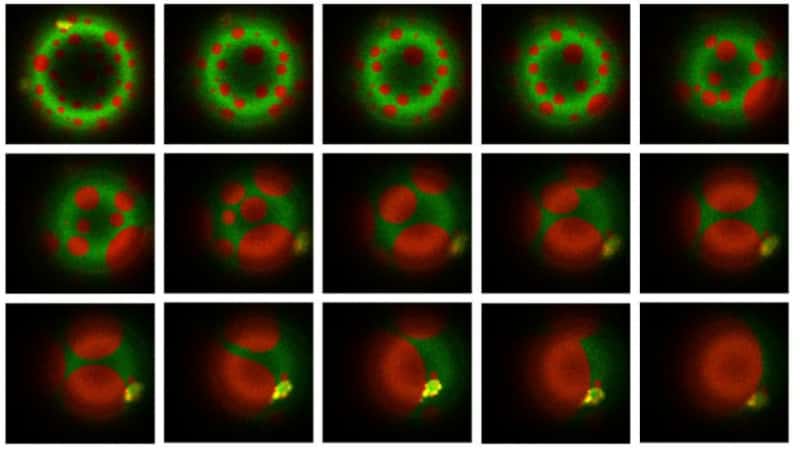

Les résultats de cette recherche, qui seront présentés lors du 70e congrès annuel de la Biophysical Society à San Francisco, du 21 au 25 février 2026, et récemment publiés sur bioRxiv, révèlent que les mycobactéries libèrent de minuscules vésicules extracellulaires qui fusionnent avec les membranes des cellules immunitaires. Ces vésicules contiennent des lipides spécifiques qui augmentent la rigidité de la membrane cellulaire.
En temps normal, lorsque les cellules immunitaires capturent des bactéries nocives, elles les enferment dans un compartiment appelé phagosome, qui fusionne ensuite avec un lysosome. Les lysosomes contiennent des enzymes digestives qui décomposent et détruisent les bactéries. Cependant, l’équipe de recherche a constaté qu’en rigidifiant la membrane du phagosome, les mycobactéries empêchent cette fusion, créant ainsi une sorte de forteresse protectrice à l’intérieur même de nos cellules.
« Si la membrane devient plus rigide, il devient beaucoup plus difficile pour le phagosome de fusionner avec le lysosome »,
Ayush Panda, ancien étudiant diplômé
Les chercheurs ont également découvert que ces vésicules n’affectent pas seulement les cellules infectées, mais peuvent également agir sur les cellules immunitaires voisines, les affaiblissant avant même qu’elles n’entrent en contact avec la bactérie.
Cette découverte est d’autant plus importante qu’elle propose un nouveau modèle pour comprendre la survie des mycobactéries. Les recherches antérieures se concentraient principalement sur les protéines perturbées par les bactéries. Cette étude adopte une approche axée sur les lipides, démontrant que l’introduction de lipides bactériens dans les membranes des cellules hôtes suffit à provoquer un dysfonctionnement immunitaire.
« La découverte la plus surprenante a été que lorsque nous avons introduit des lipides mycobactériens dans des membranes imitant le phagosome de l’hôte, nous avons observé des changements physiques considérables : les propriétés de la membrane ont été complètement modifiées »,
Ayush Panda, ancien étudiant diplômé
Les chercheurs ont également observé des effets membranaires extracellulaires similaires médiés par les vésicules chez Klebsiella pneumoniae et Staphylococcus aureus, suggérant que cette stratégie pourrait être largement répandue chez les agents pathogènes. Ces résultats ouvrent des perspectives prometteuses pour le développement de nouveaux traitements, ciblant potentiellement les protéines impliquées dans la production de ces vésicules bactériennes ou cherchant à contrer les effets de rigidification membranaire.
« Maintenant que nous comprenons comment les bactéries se protègent, nous pouvons commencer à chercher des moyens de les arrêter », conclut Panda. « Si nous parvenons à empêcher les bactéries de rigidifier ces membranes, nos cellules immunitaires pourront remplir leur rôle et éliminer l’infection. »