Publié le 16 février 2026 09h44. La Food and Drug Administration (FDA) américaine renforce ses exigences en matière de représentativité des participants aux essais cliniques, notamment pour les maladies rares, afin de garantir la crédibilité des données et l’efficacité des traitements.
- La loi FDORA (Food and Drug Omnibus Reform Act) oblige désormais les promoteurs d’essais cliniques à définir des objectifs d’inscription basés sur l’épidémiologie réelle des maladies.
- Le recrutement de participants reste un défi majeur, avec près de 30 % des sites de recherche qui ne parviennent pas à en recruter un seul.
- Un nouveau modèle, DATA (Données, Accès, Traçabilité, Advocacy), propose une approche structurée pour améliorer l’inscription et la qualité des données dans les essais sur les maladies rares.
Le développement de nouveaux traitements, en particulier pour les maladies rares, est confronté à un défi de taille : garantir que les essais cliniques reflètent fidèlement la diversité des populations touchées. Avec l’adoption de la loi FDORA en 2022, la FDA américaine a franchi une étape décisive en rendant obligatoire la définition d’objectifs d’inscription basés sur l’épidémiologie des maladies. Cette nouvelle exigence marque un tournant, car elle lie directement la crédibilité des preuves scientifiques à la représentativité des participants aux essais.
Pourtant, le recrutement de participants reste un obstacle majeur. Selon une étude récente de CSSi, près de 30 % des sites de recherche ne parviennent pas à recruter un seul participant, entraînant des retards, des réductions d’effectifs, voire des interruptions d’essais. Cette situation crée une perte importante de ressources et creuse le fossé entre les exigences réglementaires et la réalité opérationnelle.
Le problème est particulièrement aigu dans le domaine des maladies rares, où les populations de patients sont souvent petites, dispersées géographiquement et prises en charge en dehors des réseaux d’essais traditionnels. Dans des pathologies comme l’hémophilie A, où le risque de développer des inhibiteurs varie selon les populations, un recrutement insuffisant peut même biaiser l’interprétation des résultats scientifiques. Il ne s’agit plus de savoir si il faut viser une inscription représentative, mais comment la rendre réalisable et scientifiquement défendable.
Du mandat réglementaire à une approche opérationnelle
La loi FDORA clarifie les attentes de la FDA, mais laisse aux promoteurs une marge de manœuvre quant à la manière de mettre en œuvre l’inscription basée sur l’épidémiologie, en particulier dans le contexte des maladies rares. Pour les équipes de développement, cela représente un défi pratique : concevoir des stratégies d’inscription qui soient à la fois réalistes et scientifiquement rigoureuses, dans un contexte où chaque participant a une importance particulière.
Pour répondre à cette exigence, il est nécessaire de dépasser les simples tactiques de recrutement et d’adopter une approche structurée de la génération de preuves.
Le modèle DATA : une nouvelle approche
Pour passer d’une inscription axée sur la conformité à des données scientifiquement crédibles, les promoteurs ont besoin d’un cadre opérationnel concret. Le modèle DATA propose une approche scientifique pour le développement de traitements contre les maladies rares, intégrant l’épidémiologie, l’accès, la traçabilité et l’implication des associations de patients, tout en préservant l’intégrité des données. Il ne s’agit pas d’introduire de nouveaux outils, mais de réorganiser et de connecter les pratiques existantes pour répondre aux nouvelles exigences en matière d’inscription représentative et basée sur les données.
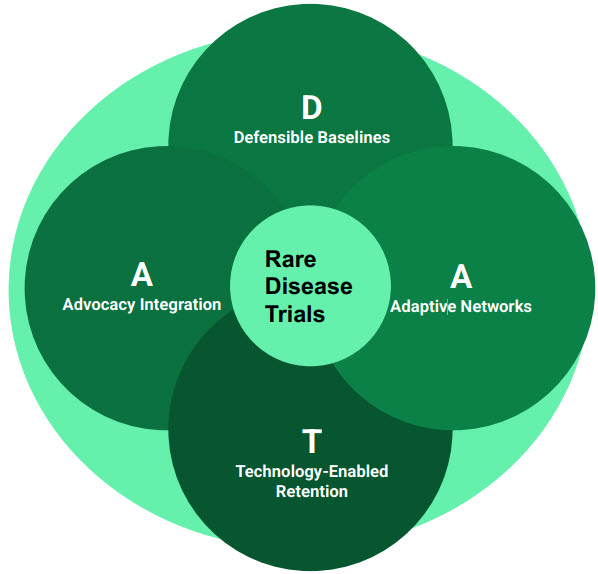
1. Établir des bases de référence solides (D) : utiliser les données du monde réel
Traditionnellement, les objectifs de recrutement ont souvent été fixés en fonction de la faisabilité plutôt que de l’épidémiologie de la maladie. Dans le domaine des maladies rares, cela a parfois conduit à des hypothèses erronées qui frustrent les équipes opérationnelles et ne reflètent pas les différences biologiques sous-jacentes. La loi FDORA change cette approche en liant explicitement les objectifs d’inscription aux données disponibles. La première étape du modèle DATA n’est donc pas la sensibilisation ou l’activation des sites, mais l’établissement de bases de référence solides à l’aide de données du monde réel (RWE).
Les RWE permettent aux promoteurs de cartographier la véritable empreinte démographique et géographique d’une maladie. Pour les troubles métaboliques rares ou les déficits enzymatiques, les populations de patients peuvent être inégalement réparties entre les régions ou concentrées dans des communautés spécifiques en raison d’effets fondateurs, de dérive génétique ou de modèles historiques de diagnostic et de soins. En exploitant les données de remboursement, les données de santé électroniques (DSE) et les registres de patients, les promoteurs peuvent définir des objectifs d’inscription qui s’alignent sur les exigences de la FDA et reflètent la biologie de la maladie. Principes des données probantes sur les maladies rares.
Cette approche permet d’élaborer des stratégies d’inscription à la fois réalistes et défendables. Lorsque les objectifs de recrutement sont fondés sur des données épidémiologiques et du monde réel, plutôt que sur des hypothèses ou des directives internes, les promoteurs renforcent la crédibilité réglementaire tout en protégeant l’intégrité scientifique.
La FDORA reconnaît également que l’inscription basée sur l’épidémiologie n’est pas toujours réalisable dans tous les contextes de maladies rares. Dans les cas où les populations sont extrêmement petites, mal caractérisées ou géographiquement limitées, les objectifs de représentativité peuvent être structurellement inatteignables, même avec une planification rigoureuse. Dans le cadre du modèle DATA, cela ne constitue pas un échec de la stratégie d’inscription, mais une conclusion tirée de celle-ci. Les bases de référence solides issues des RWE permettent aux promoteurs de démontrer quand les écarts par rapport à la représentativité reflètent des contraintes biologiques et épidémiologiques plutôt que des limitations opérationnelles, facilitant ainsi un dialogue transparent et crédible avec les autorités réglementaires.
2. Créer des réseaux adaptatifs (A) : la solution « hub-and-spoke »
Historiquement, les essais de thérapies avancées ont été concentrés dans les grands centres médicaux universitaires en raison de la complexité de l’administration de vecteurs viraux, de perfusions d’enzymes ou d’autres interventions spécialisées. Bien que cette centralisation soit souvent nécessaire pour des raisons de sécurité et de surveillance, elle peut également limiter l’accès en restreignant la participation aux patients qui vivent à proximité de ces centres, négligeant ainsi les patients éligibles pris en charge en milieu communautaire.
Pour combler cette lacune, le modèle DATA met l’accent sur les réseaux de sites adaptatifs construits autour d’une structure formelle « hub-and-spoke ». Dans ce modèle, les centres d’excellence servent de pôles de traitement, tandis que les médecins communautaires agissent comme des relais, identifiant et orientant les patients appropriés. Il est important de noter que cette approche va au-delà de la simple sensibilisation ou des références ponctuelles. Elle nécessite des partenariats opérationnels qui permettent aux hématologues communautaires, aux neurologues ou à d’autres spécialistes de fonctionner en tant que contributeurs intégrés à l’essai, même s’ils ne sont pas des sites d’investigation à part entière.
La mise en œuvre de ce modèle commence par la simplification du parcours de référence. Les médecins communautaires manquent souvent de temps et ne disposent pas de l’infrastructure nécessaire pour répondre à des critères d’éligibilité complexes ou à la logistique des études. Les promoteurs peuvent réduire ces obstacles en déployant des outils de présélection rationalisés et des ressources de support dédiées pour coordonner les références, les évaluations et le transfert des patients vers le centre approprié. En réduisant les obstacles opérationnels à la participation, les réseaux adaptatifs élargissent la portée des essais et aident à identifier des patients cliniquement éligibles mais historiquement déconnectés des parcours de recherche traditionnels.
3. Assurer la rétention grâce à la technologie (T) : penser à long terme
Dans les essais sur les maladies rares, le fardeau de la participation ne s’arrête pas à l’inscription. Les thérapies avancées nécessitent souvent un suivi à long terme pour évaluer la durabilité et la sécurité, s’étendant parfois sur une décennie ou plus. Pour les familles qui vivent à plusieurs heures d’un site d’essai, des voyages répétés pendant de nombreuses années peuvent devenir un facteur décisif dans leur décision de rester ou non dans une étude. Au fil du temps, ce fardeau contribue à une attrition différentielle, avec des conséquences sur l’exhaustivité et l’interprétabilité des données de sécurité à long terme.
La rétention technologique offre un moyen pratique de relever ce défi. Même si l’administration initiale de thérapies complexes peut nécessiter des soins hospitaliers ou des installations spécialisées, ce n’est pas le cas d’une grande partie de la surveillance ultérieure. La capture de données à distance, les consultations de télémédecine et les visites de soins infirmiers à domicile pour le prélèvement d’échantillons peuvent réduire les visites inutiles sur site sans compromettre la surveillance ou la qualité des données.
La mise en œuvre de ces outils transforme la rétention d’un obstacle logistique en une considération de conception. Remplacer les visites de routine en personne par des évaluations à distance ou un soutien infirmier mobile peut réduire considérablement le temps, les déplacements et les coûts indirects pour les participants, améliorant ainsi l’engagement à long terme dans divers contextes socio-économiques. En réduisant le fardeau d’une participation continue, les promoteurs peuvent préserver l’exhaustivité du suivi et renforcer la crédibilité des ensembles de données de sécurité à long terme – une considération de plus en plus importante à mesure que les autorités réglementaires examinent les taux d’attrition dans les études de suivi prolongées.
4. Intégrer les associations de patients (A) : un partenaire de conception du protocole
Le dernier pilier du modèle DATA est l’intégration des associations de patients. Dans le domaine des maladies rares, les associations de patients jouent un rôle central dans l’établissement de la confiance et de l’engagement. Pourtant, les équipes opérationnelles n’engagent souvent ces groupes qu’après l’apparition de problèmes d’inscription, lorsque les opportunités d’influencer la conception des études sont déjà passées.
Pour soutenir l’inscription des représentants, l’engagement avec les associations de patients doit commencer plus tôt, lors de l’élaboration du concept du protocole et du synopsis. La méfiance à l’égard des institutions médicales reste un obstacle pour de nombreuses communautés, et cette méfiance est souvent renforcée par des protocoles qui ne reflètent pas la réalité de la maladie. Des critères d’éligibilité restrictifs, des calendriers de visites rigides ou des hypothèses de base non examinées peuvent involontairement exclure des patients qui sont cliniquement représentatifs mais désavantagés sur le plan opérationnel.
L’intégration des dirigeants des associations de patients dans les premières discussions sur le protocole permet aux promoteurs d’identifier les obstacles potentiels avant qu’ils ne soient intégrés à l’étude. Des questions telles que celles de savoir si les calendriers de visite imposent un temps ou une charge économique excessive, ou si les critères d’exclusion filtrent par inadvertance des sous-populations spécifiques, peuvent être traitées de manière proactive. En intégrant cette perspective dès le départ, les promoteurs peuvent optimiser les protocoles pour soutenir l’inclusion dès la conception, ce qui renforce à la fois la faisabilité de l’inscription et la pertinence des données résultantes.
La voie à suivre
Le mandat de la FDORA n’est pas simplement un autre obstacle réglementaire ; il représente un changement de cap vers une meilleure science. À l’ère des thérapies avancées, où le bagage génétique et le contexte réel peuvent influencer de manière significative la sécurité et l’efficacité, le recrutement représentatif est indissociable de l’intégrité des données. La manière dont les patients sont recrutés dans les essais détermine désormais directement la manière dont les résultats sont interprétés, fiables et appliqués.
Pour les professionnels de la recherche clinique et les dirigeants opérationnels, le défi est de concevoir des essais aussi innovants dans leur exécution que dans leur pharmacologie. Le modèle DATA offre une voie pratique à suivre. En fondant les objectifs d’inscription sur des bases de référence solides, en élargissant l’accès via des réseaux adaptatifs, en réduisant l’attrition grâce à la rétention technologique et en intégrant les associations de patients dès le début de la conception du protocole, les promoteurs peuvent passer d’un recrutement réactif à une génération délibérée de preuves.
Dans le développement des maladies rares, où chaque participant a une importance scientifique, ce changement est essentiel. Les essais conçus dans un souci de représentativité sont mieux placés pour fournir des données auxquelles les autorités réglementaires peuvent faire confiance, que les cliniciens peuvent appliquer et que les patients peuvent reconnaître comme pertinentes par rapport à leur expérience vécue. En ce sens, la FDORA ne se contente pas de relever la barre en matière d’inscription, elle clarifie la voie vers des preuves cliniques plus crédibles, inclusives et durables dans le développement de médicaments modernes.
Références :
- Loi omnibus sur la réforme des aliments et des drogues de 2022. Section 3601-3607. Washington, DC : 117e Congrès américain ; 2022. https://www.congress.gov/bill/117th-congress/house-bill/2617/text
- CSSi. « Tendances 2025 en matière de recrutement de patients : de la perturbation à la précision. » Responsable clinique. Consulté en janvier 2026. https://www.clinicalleader.com/doc/trends-in-patient-recruitment-from-disruption-to-precision-0001
- Ahmed AE, Pratt KP et al. Race, origine ethnique, variantes F8 et risque d’inhibiteur : analyse de la base de données sur l’hémophilie A « My Life Our Future ». J Thromb Hémost. 2023;21(4):800-813. https://pubmed.ncbi.nlm.nih.gov/36696179/
À propos de l’auteur :
 Mariam Badmus est spécialiste des études cliniques et chercheuse dans l’industrie des biotechnologies, travaillant dans le développement clinique de maladies rares et génétiques. Son travail couvre les thérapies géniques, les traitements de substitution enzymatique et d’autres thérapies biologiques utilisées dans les maladies rares et génétiques. Elle se concentre sur les opérations d’essais cliniques et les considérations réglementaires pour étayer des preuves crédibles et prêtes à être soumises aux autorités réglementaires. Son expérience comprend des recherches précliniques sur des modèles de maladies rares et génétiques à l’UCSF, qui éclairent son approche translationnelle de la conception d’essais cliniques. Elle est titulaire d’une maîtrise en médecine translationnelle de l’UC Berkeley et de l’UCSF ainsi que d’une licence en pharmacie.
Mariam Badmus est spécialiste des études cliniques et chercheuse dans l’industrie des biotechnologies, travaillant dans le développement clinique de maladies rares et génétiques. Son travail couvre les thérapies géniques, les traitements de substitution enzymatique et d’autres thérapies biologiques utilisées dans les maladies rares et génétiques. Elle se concentre sur les opérations d’essais cliniques et les considérations réglementaires pour étayer des preuves crédibles et prêtes à être soumises aux autorités réglementaires. Son expérience comprend des recherches précliniques sur des modèles de maladies rares et génétiques à l’UCSF, qui éclairent son approche translationnelle de la conception d’essais cliniques. Elle est titulaire d’une maîtrise en médecine translationnelle de l’UC Berkeley et de l’UCSF ainsi que d’une licence en pharmacie.

